توسعه دارو پرخطر و طولانی است. انتظار برای درمانهای جدید بالقوه برای بیماران، بهویژه آنهایی که شرایط نادری دارند یا درمان سختی دارند، سخت است، و اگر بازار کوچک باشد، هزینه داروی تایید شده ممکن است بالا باشد. استفاده مجدد و جابهجایی داروهای موجود (همچنین به عنوان بازپروفایلینگ نیز شناخته میشود) میتواند روند را تسریع کند و سرمایهگذاری مالی مورد نیاز را در مقایسه با داروهای جدید کاهش دهد و اطمینان حاصل کند که بیماران میتوانند سریعتر و با هزینههای مقرون به صرفهتر به درمانها دسترسی پیدا کنند.[1, 2]
چهار گروه کلیدی از داروهای استفاده مجدد وجود دارد - داروهایی که به بازار عرضه می شوند تحت اختراعات موجود یا منقضی شده، داروهایی که در مراحل بالینی یا نظارتی خاتمه یافته اند، استریو ایزومرها یا متابولیت های داروهای موجود، یا نامزدهایی که در آن تغییرات جزئی در داروهای موجود ایجاد شده است. مهم است که به خاطر داشته باشید که شکست دارو در کارآزماییهای بالینی فقط به دلیل کارایی یا مسائل ایمنی ایجاد نمیشود - میتواند به این دلیل باشد که یک شرکت مسیر را تغییر میدهد، مشکلاتی در فرمولاسیون دارد، یا به این دلیل است که مشکلاتی با منافع تجاری یا برنامهریزی استراتژیک ضعیف وجود دارد.[3]
مزایای استفاده مجدد و تغییر موقعیت داروها
در حالی که این دو اصطلاح اغلب به جای یکدیگر استفاده می شوند، استفاده مجدد از دارو می تواند به مصرف یک داروی تایید شده و استفاده از آن برای نشانه دیگری اشاره داشته باشد. جابجایی دارو می تواند به شروع مجدد توسعه دارویی که متوقف شده، برای کسب تاییدیه برای نشانه جدید اشاره داشته باشد.[1]
مزایای اصلی استفاده مجدد یا تغییر موقعیت داروها جنبه هزینه و زمان است. بازه زمانی تولید یک داروی جدید معمولاً یک تا سه سال است، در حالی که میانگین 12 سال برای یک داروی جدید است.[4]
برای شرکتی که دارویی را تولید می کند که در حال توسعه متوقف شده است، یا دارویی که برای نشانه دیگری به بازار رسیده است، توانایی "بازیافت" داده های ایمنی پیش بالینی و/یا بالینی موجود، سمیت و فارماکوکینتیک/فارماکودینامیک باعث صرفه جویی در هزینه و زمان می شود. . همچنین به آنها اجازه می دهد تا پول سرمایه گذاری شده در دارویی را که در غیر این صورت ممکن است یک داروی شکست خورده باشد، جبران کنند. دانش موجود نیز خطر شکست را کاهش می دهد.
داروهایی که شکست خورده اند یا در حال توسعه نیستند، اما هنوز دارای مقداری حفاظت از حق اختراع هستند، ممکن است برای نشانه دیگری توسط شرکت سازنده یا دارنده مجوز تغییر مکان دهند. استفاده مجدد همچنین می تواند به شرکت ها اجازه دهد تا چرخه عمر داروهای عرضه شده خود را که در حال نزدیک شدن به انقضای حق ثبت اختراع هستند، تمدید کنند، زیرا می توانند از نشانه های جدید محافظت کنند. استفاده مجدد و جابهجایی داروها نیز میتواند برای شرکتهایی که داروهای بیماریهای نادر را تولید میکنند، با تشویق همکاری و به اشتراک گذاشتن دادهها و منابع ارزشمند باشد.[3, 5]
مراحل توسعه و کسب تاییدیه برای یک داروی استفاده مجدد می تواند شامل موارد زیر باشد:
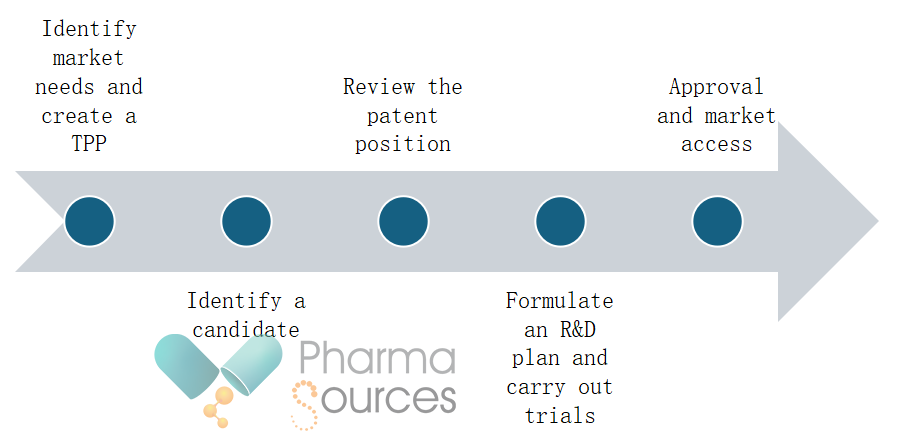
نیازهای بازار را شناسایی کنید و یک پروفایل محصول هدف ایجاد کنید
برای شرکتی که میخواهد دارویی را تغییر کاربری دهد اما نامزد موجود را در ذهن ندارد، اولین قدم این است که چشمانداز بازار را ارزیابی کند تا ببیند آیا بیمار به داروی جدید نیاز دارد و آیا شرکت قادر به جبران آن است یا خیر. سرمایه گذاری در توسعه دارو این با توسعه پروفایل محصول هدف (TPP) پشتیبانی می شود. TPP ویژگی های مورد نظر یک دارو را در حال توسعه برای یک اختلال خاص توصیف می کند. این یک راهنمای در سراسر توسعه دارو برای تمام تیم های درگیر در اختیار شرکت قرار می دهد. [2, 6, 7]
مناطق تحت پوشش TPP، که برای بررسی زمانی که یک شرکت کاندیدای خاصی را در ذهن دارد نیز مفید است، عبارتند از:[2, 7, 8]
●نشان
○نشانه هدف اولیه
○ نشانه های بالقوه آینده
●جمعیت
○بازار هدف اولیه – اولویت های اقتصادی یا حوزه هایی که بیشترین نیاز برآورده نشده را دارند
○ امکان سنجی مطالعه
○نیاز به تشخیص همراه برای شناسایی زیرجمعیتها
●هدف گیری/فارماکوکینتیک
●ایمنی، تحمل پذیری و کارایی
○نقاط پایانی مطالعه
○مزایا در مقایسه با رقبای فعلی/آینده یا استاندارد مراقبت
●تداخلات دارویی و دارویی
●ثبات
○ الزامات ذخیره سازی
○ممکن است به بازارهای هدف بستگی داشته باشد
●مسیر تجویز/فرمولاسیون
○فرمولاسیون فعلی/پتانسیل برای فرمول بندی مجدد
○کدام راه تجویز توسط بیماران ترجیح داده خواهد شد؟
○آیا دستگاه تحویل مورد نیاز است و آیا از قبل موجود است
●تکرار دوز
○در مقایسه با استاندارد مراقبت در نظر بگیرید
●هزینه
○هزینه هدف در هر دوز، بر اساس تجزیه و تحلیل چشم انداز رقابتی
●زمان تا در دسترس بودن
○زمان مورد نیاز برای آزمایشات بالینی و فرآیندهای نظارتی
○زمان مورد نیاز برای ارزیابی فناوری سلامت (HTAs)
یک نامزد را شناسایی کنید
یک شرکت ممکن است دارویی را به عنوان یک کاندیدای استفاده مجدد در ذهن داشته باشد، برای مثال یک نشانه جدید را بر اساس یافته ای که به عنوان یک عارضه جانبی در فرآیند توسعه قبلی تلقی می شود، قرار دهد.

برای شرکتی که به دنبال دارویی برای یک هدف یا نشانه خاص است، رویکردها میتوانند هدف-، ساختار-، امضا-، مسیر-، شبکه-، دانش- یا مبتنی بر دادههای بالینی باشند، با رویکردهای خاص شامل:[13-17]
● تصادفی سازی مندلی برای ایجاد روابط بین فنوتیپ ها و اثرات دارویی پیش بینی شده ژنتیکی
● داده های چند omics در مقیاس بزرگ برای درک بهتر علت شناسی بیماری و شناسایی اهداف دارویی جدید
● یادگیری ماشینی برای شناسایی زیرشاخههای بیماری و اهداف دارویی، یا پیوند آسیبشناسی و مکانیسمهای مولکولی
● هوش مصنوعی مولد یا ادغام بیان ژن انسانی، اختلالات دارویی، و دادههای بالینی، برای شناسایی نامزدها
موقعیت ثبت اختراع را بررسی کنید
شرکتی که میخواهد یک دارو را تغییر کاربری دهد یا تغییر مکان دهد، باید از موقعیت ثبت اختراع موجود، از جمله پتنتهای ترکیب اصلی، و فرمولها، رژیمهای دوز یا کاربردهای خاص آگاه باشد. اگر دارو هنوز تحت پوشش یک پتنت باشد، آنها باید با دارنده پتنت تماس بگیرند و ببینند که آیا علاقه مند به همکاری یا صدور مجوز برای دارو هستند یا خیر. اگر دارو بدون ثبت اختراع باشد، آزادی عمل بیشتری وجود دارد.[4]
همه داروها، از جمله داروهای تغییر کاربری و جایگزینی، نیاز به سطحی از حمایت از حق اختراع دارند تا به شرکتی که قصد استفاده مجدد را دارد، قبل از مواجهه با رقابت، هزینه های خود را جبران کند. انواع ثبت اختراع جدید می تواند شامل موارد زیر باشد: [4, 18]
● اندیکاسیون درمانی
●فرمولاسیون
●رژیم دوز
● سیستم تحویل
● ترکیب داروها
●ترکیب دارو/دستگاه
یک برنامه تحقیق و توسعه تدوین کنید و آزمایشات را انجام دهید
برای توسعه موفقیتآمیز یک داروی تغییر کاربری، شرکتها باید با پزشکان و یک تیم چند رشتهای متشکل از کارشناسان داخلی و خارجی برای حمایت از فرآیند توسعه کار کنند. داروهای تغییر کاربری هنوز باید داده های پیش بالینی کافی داشته باشند، آزمایشات بالینی را پشت سر بگذارند و استانداردهای دقیق نظارتی را در نشانه جدید خود رعایت کنند. در حالی که دادههای انسانی و غیرانسانی موجود از ایمنی و سمیت حمایت میکنند، مطالعات بالینی بیشتری برای تأیید اثربخشی در گروه بیمار قبل از ارسال برای تأیید مورد نیاز است.[8]کار با بیماران و گروههای حامی بیمار نیز مهم است تا بفهمیم چه چیزی از یک درمان نیاز دارند و شرکتکنندگان را برای آزمایشهای بالینی استخدام کنیم.[4]
تایید و دسترسی به بازار
همکاری نزدیک با مقامات نظارتی و نهادهای ارزیابی فناوری سلامت (HTA) از یک فرآیند کارآمد در جهت تأیید، بازاریابی و بازپرداخت حمایت خواهد کرد. مقامات نظارتی میتوانند توصیه کنند که چه آزمایشهای بالینی مورد نیاز است، و پیشنهاد کنند که کدام مسیر برای تأیید، از جمله مسیرهای تسریعشده، برای یک دارو و نشانه خاص مناسبترین است.[4]
به طور خلاصه
استفاده مجدد و جابجایی دارو راهی مقرون به صرفه و کارآمد به بازار ارائه می دهد که به بیماران امکان می دهد سریعتر به داروها دسترسی پیدا کنند. شرکتها باید مطمئن باشند که دادههای مناسب را برای یک فرآیند روان جمعآوری میکنند، و این میتواند با همکاری با بیماران، سایر شرکتها، مقامات نظارتی و نهادهای ارزیابی فناوری سلامت کمک کند.
مراجع
1. Bakker، A.، یک مسئله معنایی به ظاهر کوچک، مانع اصلی برای توسعه درمان برای بیماریهای نادر است. STAT، 2023. موجود از: https://www.statnews.com/2023/06/27/drug-repurposing-repositioning-rare-diseases/.
2. Griffiths, A., et al., Target Product Profiles in Pharmaceutical Development KPMG. 2023. موجود در: https://assets.kpmg.com/content/dam/kpmg/uk/pdf/2023/01/target-product-profiles-in-pharmaceutical-development.pdf.
3. الویدج، اس.، بیرون آوردن جن تغییر موقعیت دارو از بطری. Life Science Leader، 2010. موجود در: https://www.lifescienceleader.com/doc/getting-the-drug-repositioning-genie-out-of-the-bottle-0001.
4. پیسانی، ج.، و همکاران، استفاده مجدد از داروها: فرصت و چالش. 2021. موجود از: https://www.lifearc.org/wp-content/uploads/2024/03/RD-Drug-repurposing-report.pdf.
5. Taylor, M., M. Salova, and A. Schroeder, Drug Repurposing: Potential to Expand Rare Disease Treatment. Avalere: Insights & Analysis، 19 فوریه 2024. موجود در: https://avalere.com/insights/drug-repurposing-potential-to-expand-rare-disease-treatment.
6. کارمند نویس. پروفایل های محصول را هدف قرار دهید سازمان بهداشت جهانی. 9 ژوئیه 2024. موجود از: https://www.who.int/observatories/global-observatory-on-health-research-and-development/analyses-and-syntheses/target-product-profile/who-target-product -پروفایل ها
7. کارمند نویس. استفاده مجدد از دارو: ملاحظات کلیدی شبکه های نوآوری درمانی UCL - UCL - دانشگاه کالج لندن. 9 ژوئیه 2024. موجود در: https://www.ucl.ac.uk/ion/translation-enterprise/tailored-support-translational-researchers/re-purposing-drug/repurposing-drug.
8. کارمند نویس. Repurposing Medicines Toolkit - راهنمایی برای پیمایش فرآیند. LifeArc / شورای تحقیقات پزشکی. 11 جولای 2024. موجود در: https://www.repurposingmedicines.org.uk.
9. میزگرد ترجمه تحقیقات مبتنی بر ژنوم برای سلامت، هیئت سیاستگذاری علوم بهداشتی، و مؤسسه پزشکی، در تغییر منظور و تغییر مکان دارو: خلاصه کارگاه. 2014: واشنگتن (دی سی).
10. Ghofrani، HA، IH Osterloh، و F. Grimminger، سیلدنافیل: از آنژین صدری تا اختلال نعوظ تا فشار خون ریوی و فراتر از آن. Nat Rev Drug Discov، 2006. 5 (8): ص. 689-702.
11. گوهل، دی، و همکاران، سیلدنافیل به عنوان یک داروی کاندید برای بیماری آلزایمر: مشاهده داده های بیمار در دنیای واقعی و مشاهدات مکانیکی از نورون های مشتق شده از سلول های بنیادی پرتوان القاء شده توسط بیمار. J Alzheimers Dis، 2024. 98 (2): ص. 643-657.
12. گروه مشاوره داروهای Dorset، راهنمای مراقبت مشترک برای سیلدنافیل برای مدیریت پدیده RAYNAUDS ثانویه مرتبط با اسکلروز سیستمیک NHA. 2017. موجود در: https://nhsdorset.nhs.uk/Downloads/aboutus/medicines-management/Shared%20Care%20Guidelines/Sildenafil%20Shared%20Care%20Documented%20July%2017.pdf.
13. وانگ، ال.، و همکاران، چشم انداز روش در استفاده مجدد دارو با استفاده از داده های ژنومی انسانی: یک بررسی سیستماتیک. Bioinform مختصر، 2024. 25(2).
14. Sperry، M. and DE Ingber، Drug Repurposing Strategies, Challenges and Successes. 4 مارس 2024. موجود در: https://www.technologynetworks.com/drug-discovery/articles/drug-repurposing-strategies-challenges-and-successes-384263#D3.
15. رودریگز، اس.، و همکاران، یادگیری ماشینی کاندیدهایی را برای استفاده مجدد از دارو در بیماری آلزایمر شناسایی می کند. Nat Commun, 2021. 12(1): p. 1033.
16. Yan, C., et al., Leveraging AI مولد برای اولویت بندی نامزدهای استفاده مجدد از دارو برای بیماری آلزایمر با اعتبار بالینی در دنیای واقعی. NPJ Digit Med, 2024. 7(1): p. 46.
17. Wu, P., et al., ادغام بیان ژن و داده های بالینی برای شناسایی نامزدهای استفاده مجدد از دارو برای هیپرلیپیدمی و فشار خون بالا. Nat Commun, 2022. 13(1): p. 46.
18. Conour, J., چرا روش درمان پتنت برای داروهای تغییر کاربری ارزش سرمایه گذاری را دارد؟ JD Supra: News & Insights، 5 اکتبر 2020. موجود در: https://www.jdsupra.com/legalnews/why-method-of-treatment-patents-for-92813/.

